LifeSignals 就其 LifeSignals LX1550 多參數遠端監控平台獲得 FDA 510 (k) 批准
進一步確定在醫院和家居提供持續遠端患者生命體徵監測的能力。
加州費利蒙2021年7月28日 /美通社/ – LifeSignals Inc. 今天宣佈剛就其 Lifesignals LX1550 多參數遠程監控平台獲得 FDA 2 級 510 (k) 批准。這是繼最近 CE 標記後,進一步確定 LifeSignals 建立創新無線平台的動力,臨床醫生可在家居和醫護環境中持續收集患者的生理數據。
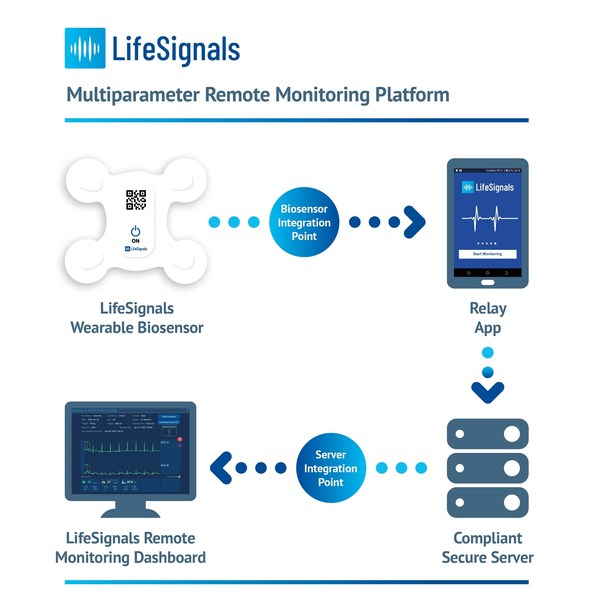
平台的核心是一個單次使用的可穿戴多參數生物感應器,可記錄心電圖(2 通道心電圖)、心率、呼吸率、皮膚溫度和身體姿勢數據長達五天。然後,加密的生理數據可透過生物感應器的高可靠功能從中繼應用程式傳送至安全的雲端平台。臨床醫生和護理供應商可存取雲端遠端監控主控頁,以查看患者的生理數據和管理提示設定。
遠端監控平台旨在讓健康科技公司能夠快速增強其產品和服務組合,從任何地點為最廣泛的患者提供生命體徵監測。中繼應用程式和主控頁方便開發人員使用,配備可隨時部署的軟件開發套件 API,也適用於大規模實施。
創辦人兼行政總裁 Surendar Magar 表示:「2019 新型冠狀病毒打破了全球遠端患者監控的障礙,我為 LifeSignals 團隊在如此短的時間內迅速作出回應而感到自豪。這項 FDA 510 (k) 批准標誌著公司發展和使命的另一個重要里程碑。產品已在印度監測 2019 冠狀病毒病患者的醫院中成功實施,並陸續在歐洲、英國、新加坡和菲律賓推出。我們現在的重點是迅速向希望擴展服務並改善患者護理的美國健康科技公司推出低成本遠端生命體徵監測功能。」