南京2020年11月4日 /美通社/ — 作為先聲藥業「自主研發+國際合作」雙輪驅動的成果之一,今年8月先聲藥業剛從美國G1 Therapeutics買下Trilaciclib獨家許可,先聲享有該藥物大中華地區(中國大陸,香港,澳門和台灣地區)所有適應症的開發和商業化權益。儘管在中國尚在臨床前階段,但Trilaciclib在美國已經是FDA認定的突破性療法,並很有希望在2021年獲批上市,其首個適應症為減輕小細胞肺癌的化療副作用。該項目的三大硬核屬性不可小覷。
一、全新機制,美國突破性療法認定
CDK 4/6(細胞週期蛋白依賴型激酶4/6)為近幾年來全球炙手可熱的抗癌小分子藥靶點。作為調控細胞週期從G1期向S期分化的重要開關,CDK 4/6被特異性阻斷可抑制腫瘤細胞的複製。從國際廠商輝瑞、諾華到國內廠商恆瑞、貝達……各大藥企紛紛開發CDK 4/6抑制劑,適應症主要集中在CDK 4/6過度活躍的ER+乳腺癌。
有意思的是,Trilaciclib雖同為CDK 4/6抑制劑,卻是一種first-in-class藥物,其以獨特機制降低化療副作用,並且首個適應症為小細胞肺癌(SCLC)。
SCLC在腫瘤界以難治著稱,該腫瘤細胞對CDK 4/6依賴度低,普通CDK 4/6抑制劑對其依然無可奈何。
Trilaciclib開發策略卻恰好針對這一點,並非抑制癌細胞,而是作為CDK 4/6短效而可逆的抑制劑,在化療前作用於需要受保護的正常人體組織 — 骨髓造血干細胞。使得骨髓細胞分裂期暫停在G1期不向DNA合成的S期發展,從而避免被化療殺死。此時對CDK 4/6抑制劑不敏感的腫瘤細胞已然全面進入S期後被化療殺死。
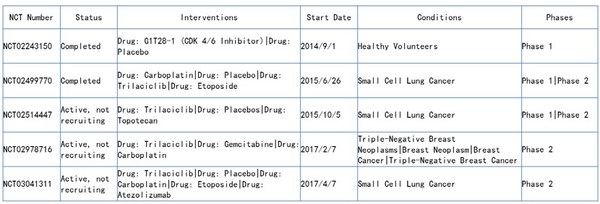
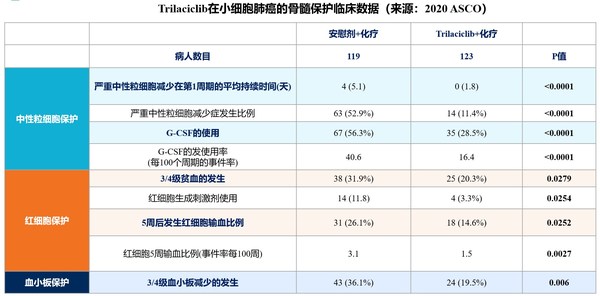
目前,Trilaciclib已開展三項針對小細胞肺癌的隨機、雙盲、安慰劑對照臨床試驗,患者在接受化療前給予trilaciclib治療,相對於安慰劑組,Trilaciclib大大改善了患者體驗:尤其顯著減少了疲勞,減少中性粒細胞減少症、貧血和血小板減少症,減少了G-CSF的使用和輸血。
基於令人信服的骨髓保護效果數據,Trilaciclib於2019年被FDA認定為「突破性療法」,並躋身優先評審的快速通道,目前已向FDA提交了新藥上市申請(NDA),有望於2021年在美國獲批。
二、三陰乳腺癌&more
除小細胞肺癌外,Trilaciclib另一項亮眼的成績在於顯著提升三陰性乳腺癌的生存獲益(OS)。三陰性乳腺癌是層出不窮的免疫靶向療法洪流中著名的孤島。因缺乏敏感靶點,除傳統化療以外,可用藥物寥寥無幾。
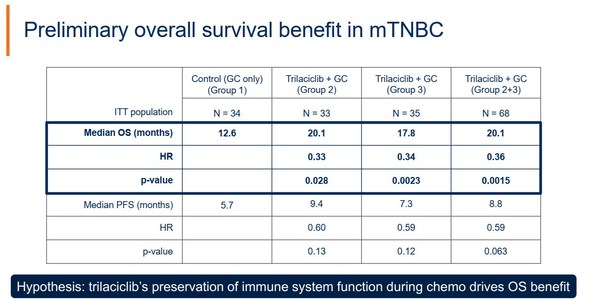
一項 II期臨床試驗(NCT02978716)顯示,Trilaciclib與卡鉑和吉西他濱(GC治療)聯用,使患者可以耐受更多的化療週期,減少了輸血率;患者的OS綜合較安慰劑組延長7.5個月,具有統計學意義;患者的PFS也有所改善。
強大的數據結果使得Trilaciclib也有望成為三陰性乳腺癌治療的突破。此外,化療依然是當前幾乎所有腫瘤治療的基石療法,作為化療減毒藥物,理論上Trilaciclib可用於所有化療的輔助保護用藥。
可以想像,未來一旦上市,Trilaciclib的競爭對手也不是其他CDK4/6抑制劑,而是集落刺激因子、促紅細胞生成素(EPO)、血小板生長因子以及用於化療保護、生血的中藥方劑等各類用於化療輔助支持用藥。
如果把化療比喻為一場地震,相比目前市面上各類化療後升紅、升白藥物在骨髓受損後再去補救性刺激造血(災後重建),Trilaciclib則有望預防性給藥,使得骨髓細胞在化療中免於受損(預先抗震防災),優勢不言而喻。
目前,單是最常用的化療後升白藥粒細胞集落刺激因子(G-CSF)一項,2019年全球市場規模近60億美元。最重要的促紅細胞生長因子EPO藥品全球銷售額在2006年時達到峰值126億美,目前隨著競爭降價而逐漸回落至70億美元。Trilaciclib的分子機制,使其有潛力在腫瘤輔助用藥領域搶佔和取代眾多化療保護和升血藥物市場,市場潛力巨大。
三、開發資源完備,有望快速引進中國
先聲藥業是中國一家具有完備的研發生產銷售全流程的綜合集團型藥企,無論是自主研發或對外乃至跨國合作研發,都已有多個已上市新藥的成功先例。該公司與跨國藥企BMS合作引進中國的類風關重磅藥物阿巴西普(2019年全球銷售額32億美元)剛在今年獲批上市,佐證了先聲在臨床開發上的實力,以及BMS對其商業化能力的認可。
獲得Trilaciclib大中華區所有適應症的獨家權益,是一樁被業界盛讚的聰明deal。而先聲的臨床開發團隊也有能力和足夠的學術、政策資源把這款新藥在臨床進度上快速推進。
據先聲藥業港交所上市招股書信息,Trilaciclib的中國I期臨床有望在2021年3季度啟動。而這款現在美國優先審評的藥物屆時或已在美國上市,屆時更多的臨床數據出爐,將更有利於項目在中國落地並走上商業化,或進入快速審評通道,早日讓更多患者受益。
綜上,一款有趣有料的first-in-class藥物Trilaciclib雖在中國尚未進入臨床,但鋒芒已現。Trilaciclib在腫瘤治療領域的潛力令其在先聲研發管
線中尤為突出,未來值得期待。